I. Panoramica di uESMOLinea guida 2025
In Aostu 2025, l'ESMO hà publicatu ufficialmente a Guida di Pratica Clinica ESMO per u Cancru di u pulmone micca à piccule cellule precoce è lucalmente avanzatu per a diagnosi, u trattamentu è u seguitu, publicata in a principale rivista oncologica Annals of Oncology. Questa hè a prima aghjurnazione cumpleta dapoi a versione 2017 è furnisce una riferenza estremamente autorevole per l'oncologi di u mondu sanu.

U cancru di u pulmone hà a più alta incidenza è mortalità di tutte e malignità in u mondu. Ogni annu, ci sò più di 2,2 milioni di novi casi è più di 1,8 milioni di morti, ciò chì face di u cancru di u pulmone a principale causa di morte ligata à u cancru sia in l'omi sia in e donne. U cancru di u pulmone à cellule micca chjuche (NSCLC) rapprisenta circa l'80-85% di tutti i pazienti cun cancru di u pulmone. In questu cuntestu seriu, a publicazione di e linee guida di u 2025 inietta un novu impulsu scientificu in a pratica clinica, cù l'aghjurnamentu di e strategie di test di i biomarcatori chì hè particularmente criticu.
II. Interpretazione di l'aghjurnamenti chjave di e linee guida
2.1 Test di biomarcatori: da "opzionale" à "essenziale"
A linea guida di u 2025 face un aghjustamentu strategicu impurtante in quantu à i testi di biomarcatori. A linea guida dichjara esplicitamente chì i testi di biomarcatori sò essenziali per a decisione di trattamentu in i pazienti cun NSCLC di stadiu IB-III.
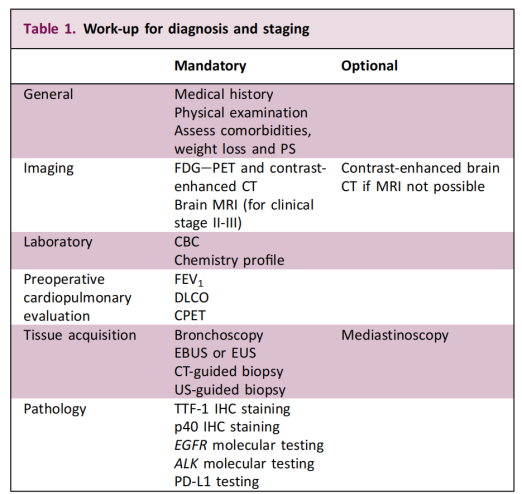
Questa raccomandazione estende i testi moleculari da a so focalizazione precedente nantu à i pazienti cun malattia avanzata à i casi in fase iniziale, resecabili. L'ughjettivu principale hè di identificà e mutazioni di i geni driver è di furnisce una basa scientifica per un trattamentu di precisione persunalizatu. A linea guida mette ancu in risaltu chì a fattibilità di a biopsia è di l'approcciu diagnosticu devenu esse determinati da una squadra multidisciplinare basata nantu à e caratteristiche di u paziente è di u tumore.
In quantu à a strategia specifica di test, a linea guida ricumanda chjaramente chì i test genetichi sianu realizati prima di a presa di decisione chirurgica, è chì devenu almenu copre EGFR è ALK. Stu cuncettu di "test in anticipu" hà una prufonda significazione clinica per a stratificazione precisa è u trattamentu persunalizatu di u NSCLC in stadiu iniziale - a puntualità è l'accuratezza di i risultati di i test determinanu direttamente a scelta di a terapia adiuvante successiva.
2.2 Sviluppi terapeutici in u NSCLC in fase iniziale pusitivu à u Driver-Oncogene
A linea guida di u 2025 integra evidenze da parechji studii clinichi maiò per stabilisce una via di trattamentu di precisione chjara per i pazienti cun NSCLC in stadiu iniziale pusitivu per l'oncogene di u driver.
Pazienti cun mutazione positiva di EGFR:Basatu annantu à u studiu ADAURA, l'osimertinib adiuvante postoperatoriu per trè anni hè diventatu u standard mundiale di cura per i pazienti cun delezioni di l'exone 19 di l'EGFR o mutazioni di l'exone 21 L858R. U studiu ADAURA hè un studiu di fase III internaziunale, multicentricu, randomizatu è cuntrullatu chì valuta l'efficacia è a sicurezza di l'osimertinib adiuvante in pazienti cun NSCLC di stadiu IB-IIIA cù mutazione EGFR cumpletamente resecatu. U studiu hà dimustratu chì osimertinib hà migliuratu significativamente sia a sopravvivenza senza malattia sia a sopravvivenza generale paragunatu à u placebo, stabilendu osimertinib cum'è u novu standard di cura per sta pupulazione. Tuttavia, l'analisi esplorative di u studiu ADAURA anu indicatu chì circa u 36% di l'interruzioni precoci di u trattamentu sò state guidate da eventi avversi, è un altru 31% eranu dovuti à a decisione di u paziente. Questa scuperta mette in risaltu a necessità di test di basa precisi prima di u trattamentu per assicurà chì a terapia mirata sia data à i pazienti chì ponu ottene un benefiziu sustenutu.
Pazienti ALK-pusitivi:Basatu annantu à a prova ALINA, l'alectinib adiuvante postoperatoriu per dui anni hè avà u standard di cura. In l'analisi primaria di a prova ALINA randomizzata in apertu di fase III, alectinib hà mostratu un benefiziu marcatu di sopravvivenza senza malattia in a pupulazione di stadiu II-IIIA, cù un rapportu di risicu di 0,24. I dati aghjurnati di a prova ALINA presentati à u cungressu ESMO 2025 anu mostratu chì dopu à ≥3 anni di seguitu, u benefiziu DFS di alectinib hè restatu "sostenutu è clinicamente significativu", cù un rapportu di risicu di 0,36 in a pupulazione di stadiu II-IIIA. L'ultimu tassu di sopravvivenza generale à 4 anni riportatu hà righjuntu u 98,4%, u tassu DFS à 4 anni era di 75,5%, è ancu a DFS di u sistema nervosu centrale hè stata migliurata, senza novi segnali di sicurezza. Quessi dati robusti stabiliscenu ulteriormente alectinib adiuvante cum'è u standard di cura dopu a resezione di NSCLC ALK-positivu è sottolineanu u valore di testi accurati per identificà tali pazienti.
Scelta di u metudu di prova:A linea guida ESMO 2025 elenca esplicitamenteanalisi di pannelli RT-PCR multiplexà fiancu à NGS, IHC è FISH basati nantu à l'ARN cum'è unu di l'approcci tecnichi raccomandati per a rilevazione di a fusione ALK. Questu indica chì u requisitu principale di a linea guida hè di realizà testi per guidà e decisioni cliniche, piuttostu chè di impone una piattaforma di test specifica. Per i prudutti RT-PCR focalizati nantu à a rilevazione di EGFR è ALK, sta strategia di test flessibile furnisce una forte ghjustificazione basata nantu à e linee guida per u so usu in a pratica clinica.
III. Soluzioni Tecniche di Test di Precisione
A linea guida di u 2025 avanza i testi versu a fase di decisione preoperatoria, ciò chì alza u livellu di precisione, sensibilità è accessibilità di i test. I dui prudutti di rilevazione basati nantu à RT-PCR descritti quì sottu sò in linea cù i requisiti di a linea guida da un puntu di vista tecnicu.
Kit di rilevazione di mutazioni 3.1 EGFR - Piattaforma tecnologica ARMS migliorata
Tecnulugia di basaA tecnulugia ARMS migliorata permette l'amplificazione specifica di sequenze mutanti à bassa abbundanza contr'à un sfondate di tipu salvaticu elevatu
Trè salvaguardie tecniche:
-ARMS miglioratu → migliora u ricunniscimentu di e mutazioni
-Arricchimentu enzimaticu → digerisce u fondu di tipu salvaticu è arricchisce e sequenze mutanti
-Bloccu di temperatura → sopprime l'amplificazione non specifica
PrestazioneSensibilità diFrequenza di l'allele mutante à 1%
Cuntrollu di a contaminazioneCuntrollu internu integratu + enzima UNG impediscenu a contaminazione
Tempu di rispostaFunziunamentu à tubu chjusu, circa120 minuti
Compatibilità di u campione:Tissutu/biopsia liquidacampioni → risponde à l'esigenza di "test in anticipu"
Cupertura:45 mutazioniin l'esoni 18-21 di EGFR, chì currispondenu precisamente à e regioni evidenziate da e linee guida (delezioni di l'exone 19 è di l'exone 21 L858R)
Usu clinicuGuida direttamente a terapia EGFR-TKI
Kit di rilevazione di fusione 3.2 MMT EML4-ALK - Soluzione di rilevazione di fusione basata su RNA

-Piattaforma tecnologicaRT-PCR basata nantu à l'ARN - offre vantaghji inerenti rispetto à i metudi basati nantu à u DNA per a rilevazione di a fusione
-Vantaghju basatu annantu à l'ARNRileva direttamente i trascritti di fusione espressi, evitendu efficacemente i falsi negativi
-Evidenza di studiuIn fusioni ALK à bassa abbundanza, RT-PCR hè significativamente più affidabile chè i testi basati nantu à u DNA.
-SensibilitàDetecta fusioni finu à20 copie per reazione
-Cupertura di e varianti: Coperture12 varianti cumuni di fusione EML4-ALK(cumprendu a variante 1 ~33%; varianti 3a/3b inseme ~29%)
-Cuntrollu di l'operazione è di a contaminazioneTubu chjusu, ~120 minuti; cuntrolli di prucessu integrati + enzima UNG impediscenu risultati falsi
-Compatibilità di u strumentuCompatibile cù diversi strumenti PCR in tempu reale mainstream
-Allineamentu di e linee guidaAltamente coerente cù a linea guida ESMO
IV. Coerenza trà i saggi è e raccomandazioni di e linee guida
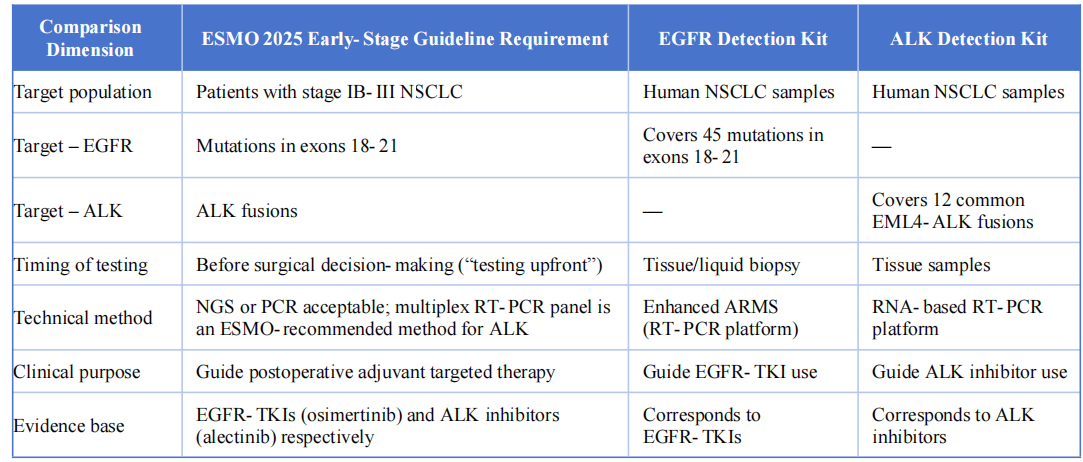
I dui prudutti di rilevazione sò assai coerenti cù a linea guida ESMO 2025 Precoce è localmente avanzatu di u cancru di u pulmone non à piccule cellule in e seguenti dimensioni chjave:
V. Cunclusione
A linea guida ESMO 2025 per u NSCLC in fase iniziale apre una nova era di diagnosi è trattamentu di precisione, centrata nantu à "testi in anticipu, targeting precisu è ottimizazione di u trattamentu."U Kit di Detezione di Mutazione EGFR è u Kit di Detezione di Fusione MMT EML4-ALK rispondenu à i requisiti di e linee guida per i miri, u timing è a precisione attraversu percorsi tecnichi distinti."
U kit EGFR usa a tecnulugia ARMS mejorata per a rilevazione ad alta sensibilità di mutazioni mirate in campioni limitati, supportendu sia a biopsia tissutale sia quella liquida per permette "test in anticipu".
U kit ALK hè basatu annantu à RT-PCR basata annantu à l'ARN, chì offre vantaghji annantu à i metudi di DNA per a rilevazione di a fusione, in cunfurmità cù a raccomandazione di l'ESMO di pannelli RT-PCR multiplex per i testi ALK.
Inseme, sti dui prudutti formanu una suluzione di test di precisione conforme à a linea guida ESMO 2025, chì sustene a terapia adiuvante persunalizata per u NSCLC in stadiu iniziale.
Referenze:
- Zer A, Ahn MJ, Barlesi F, et al. Cancru di u pulmone micca à piccule cellule precoce è lucalmente avanzatu: Linea guida di pratica clinica ESMO per a diagnosi, u trattamentu è u seguitu. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Data di publicazione: 06 di maghju 2026

